
ژرفای درد: درسی که فلفلهای تند درباره درد به ما میدهند
دیوید جولیوس (David Julius) درد را میشناسد. این پروفسور فیزیولوژی در دانشکده پزشکی دانشگاه کالیفرنیا، سانفرانسیسکو، پژوهشهای خود را وقف این کرده که سیستم عصبی چگونه درد را حس میکند و چگونه موادی مثل کپسایسین ...
دیوید جولیوس (David Julius) درد را میشناسد. این پروفسور فیزیولوژی در دانشکده پزشکی دانشگاه کالیفرنیا، سانفرانسیسکو، پژوهشهای خود را وقف این کرده که سیستم عصبی چگونه درد را حس میکند و چگونه موادی مثل کپسایسین (capsaicin) ــ ترکیبی شیمیایی که باعث تندی فلفل میشود ــ گیرندههای درد را فعال میکنند. او در سال ۲۰۱۹ به خاطر «کشف مولکولها، سلولها و مکانیسم احساس درد» موفق به دریافت «جایزه دستاورد» ۳ میلیون دلاری در زمینه علوم حیات شد.
جولیوس و همکارانش نشان دادند که چگونه پروتئینهای غشای سلول به اسم کانالهای بالقوه گیرنده گذرا (یا کانالهای TRP) در درک درد و گرما یا سرما، و همچنین التهاب و بیشحساسیت، نقش دارند. بخش بزرگی از کار او روی مکانیسمی تمرکز دارد که کپسایسین اثر قدرتمند خود را به سیستم اعصاب انسان اعمال میکند.
تیم او گیرنده حساس به کسپایسین، TRPV1، را شناسایی کردند و نشان دادند که این گیرنده از طریق گرما و مواد شیمیایی التهابزا نیز فعال میشود. او به تازگی نشان داده که چگونه سم عقرب گیرنده «واسابی» TRPV1 را هدف قرار میدهد. توسعهدهندگان دارو در حال حاضر در حال بررسی این هستند که آیا میتوان این گیرندهها را برای ساخت مسکنهای غیر اپیوئیدی مورد هدف قرار داد یا خیر.
جولیوس علاوه بر سافتههایش درباره درد، گیرندهای را کشف کرده که مسئول سیگنال مغزی سروتونین است. او همچنین به دیگر گیرندههای حسی، نظیر حس مادون قرمز در مارها و الکتروگیرندهها در مارها و سفرهماهیها، علاقه دارد.
وبسایت Scientific American با جولیوس درباره پژوهشهای او در زمینه احساس درد، نیاز ما به آن و این که درد چطور میتواند از هدف خود منحرف شود، مصاحبه کرده است.

چگونه برای اولین بار به مطالعه درد علاقمند شدید؟
وقتی در حال انجام کار پست دکتری خود بودم، به سیستم عصبی علاقه پیدا کردم. من به فهم این که انتقالدهندههای عصبی چگونه در مغز کار میکنند، و گیرندههای این انتقالدهندهها چه شکلی داشتند و به استفاده از علم ژنتیک و بیولوژی مولکولی برای فهم بخشی از این پرسشها علاقمند شدم. من بسیار مجذوب ایده پزشکی و سلامت سنتی و این که دانشمندان چگونه از محصولات طبیعی برای فهم فیزیولوژی استفاده میکنند، شدم. من به سوالاتی در مورد چگونگی عملکرد مواد توهمزا علاقه پیدا کردم ــ این که مردم چگونه چیزهایی مثل پیوت را کشف و از آن در به طور آیینی استفاده میکنند. البته که شیمیدانان اجزای فعال این مواد و چگونگی عملکرد آنها روی سیستم عصبی را کشف کرده بودند. من اما واقعا شیفه کل این رویکرد بودم، که در آن افراد برخی از رفتارهای انسانی را مطالعه میکنند و آن را به حوزه شیمی میآورند و سپس از آن مواد شیمیایی به عنوان راهنمایی برای فهم چگونگی کار سیستم عصبی انسان استفاده میکنند. همه اینها در نهایت باعث شد تا بپرسم چگونه برخی از این عاملها در محیط زیست ما باعث ایجاد درد میشوند ــ موادی مثل کپسایسین و واسابی. این برای من نوعی سیر طبیعی بود که از علاقه به استفاده از محصولات طبیعی به فهم سیستم عصبی برسم.
گویا ایده مطالعه روی کپسایسین در یک سوپرمارکت به ذهن شما رسید. چطور چنین چیزی اتفاق افتاد؟
من در قفسهها دنبال سس فلفل تند بودم و با خودم فکر میکردم «این یک مساله بسیار مهم و سرگرمکننده است. باید دربارهاش جدی باشم.» همسر من ــ او نیز یک دانشمند است ــ به من نگاه کرد و پرسید «داری چه میکنی؟» و من گفتم «واقعا گیج شدهام. باید بفهمم چطور این مساله را حل کنم.» و او گفت «پس دست از تلف کردن وقت بردار.» این مساله نیز مثل هر چیز دیگری بود: باید زمان مناسب، افراد مناسب و تکنولوژی مناسب فرا برسد. و مایکل کاترینا (Michael Caterina)، همکار آن زمان من در آزمایشگاه، کسی بود که گفت «آره، من این چالش را بر عهده میگیرم.» و تلاش خارقالعادهای انجام داد. میدانید که روش علم همین است: در لحظه درست، همه چیز جور میشود.
شما و همکارانتان کشف کردید که کپسایسین گیرندهای به نام TRPV1 را فعال میکند. این چطور در احساس در به ما کمک میکند؟
این گیرنده یک پروتئین روی سطح سلولهای عصبی است. اکثرا روی سلولهای عصبی مرتبط با احساس درد یافت میشود. این گیرنده یک کانال یونی است که شکلی مثل «دونات» دارد، و سوراخ مرکزی تا زمانی که چیزی آن را فعال کند، بسته است. سپس یونها (غالبا یونهای سدیم و کلسیم) از بیرون سلول به داخل روانه میشوند. وقتی چنین چیزی رخ میدهد، جریان الکتریکی در سلول ایجاد و فرایند پتانسیل عمل آغاز میشود. در نتیجه سینگالی الکتریکی از پیرامون ــ برای مثال لب شما که فلفل را لمس کرده ــ به سمت نخاع ارسال میشود. سپس در نخاع، نورونها (که ما به آن نورونهای حسی و گیرندههای درد انتقالی اولیه میگوییم) سیگنال را به نورون ثانویهای در نخاع میفرستند. به همین ترتیب، از طریق سلسلهای از نورونها، سیگنال به مغز و به مراکزی میرسد که از طریق آنها شما درد یا سم را حس میکنید.
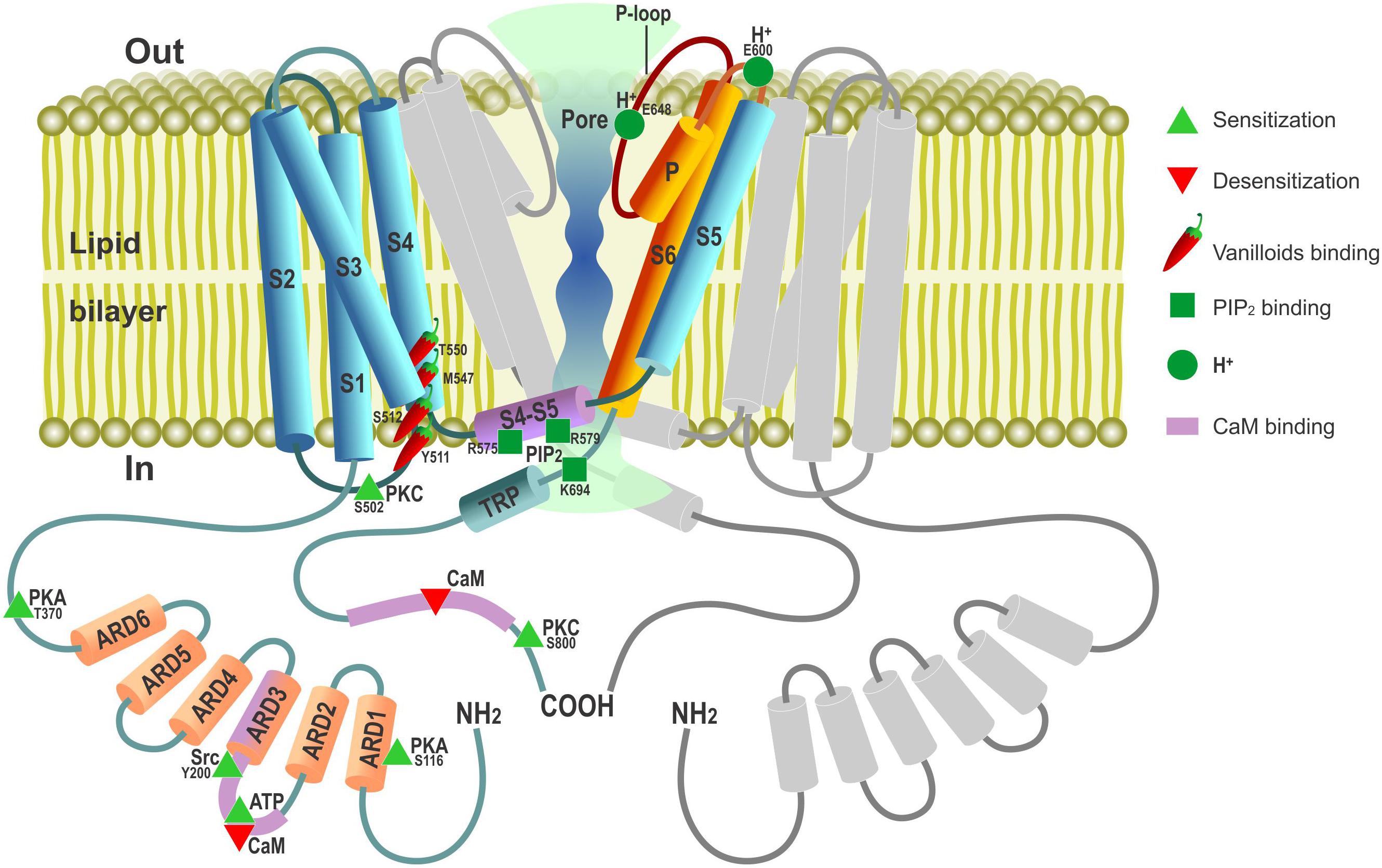
چیز جالب در مورد این کانال یونی این است که با گرما فعال میشود، در نتیجه نقشی را در توانایی ما برای احساس چیزهای داغ ایفا میکند. پس این در واقع گونهای از همگرایی اطلاعات است و یک فلفل تند محرکههای گرمایی را تقلید میکند. اما این کانال عاملهایی را که بدن ما در واکنش به التهاب ایجاد میکند نیز شناسایی میکند.
چرا ما توانایی احساس درد داریم؟
یکی از چیزهای جالب که درباره درد میدانیم این است که وقتی یک آسیب دیدگی وجود داشته باشد ــ آسیب به بافت، التهاب یا آسیب به خود تارهای عصبی ــ معمولا درد نیز بالا میگیرد. و به نظر میرسد که دلیل آن افزایش مراقبت است: وقتی مچ پایتان پیچ میخورد باید بدانید کار بدی انجام دادهاید تا بتوانید از آن محافظت کنید و اجازه دهید تا خوب شود. افرادی که این توانایی را ندارند ــ مثلا افرادی با دیابت یا جذام (بیماری هانسن) ــ احساسی در اعضای بیرونی خود ندارند. اگر آنها جراحتی در پای خود داشته باشند، آن را احساس نمیکنند و نمیدانند که باید از خود محافظت کنند، در نتیجه، زخمشان عفونت میکند. پس این افزایش احساس درد برای حفاظت از ماست و این که بدانیم باید آن نقطه را پوشش دهیم. البته برخی اوقات این مساله از کنترل خارج میشود و ما سندروم درد مزمن یا دائمی داریم.
چگونه میتوانیم از گیرنده کپسایسین و دیگر گیرندهها برای درمان درد استفاده کنیم؟
TRPV1 فقط درد را حس نمیکند؛ این گیرنده بسیاری از مواد شیمیایی را که در طول التهاب تولید میشوند نیز حس میکند. این مواد شیمیایی روی این تارهای عصبی حسکننده درد مینشینند تا حساسیت خود را به چیزهایی مثل دما، لمس و دیگر مواد شیمیایی، به عنوان بخشی از واکنشهای حفاظتی، بهبود دهند. کانال TRPV1 میتواند بسیاری از عاملهای التهابی متفاوت را شناسایی و در نتیجه در افزایش حساسیت تار عصبی نسبت به زمینه آسیب مشارکت کند. و این تقریبا تمام دلیلی است که دانشمندان به این نوع مولکولها به عنوان نقاطی بالقوه برای مسکنها علاقمند هستند: چون این مولکولها در هنگام آسیب در ایجاد درد مزمن مشارکت دارند. پس میتوانید تصور کنید در شرایطی مثل آرتروز، التهاب مثانه یا التهاب دستگاه گوارشی، که با تولید واسطههای التهابی بسیار همراه هستند، TRPV1 و دیگر کانالها بازیگران مهمی در تنظیم دوباره حساسیت تار عصبی در زمینه آسیب هستند. کاری که میخواهید انجام دهید این است که درد ناشی از آسیب را کاهش دهید. اما نمیخواهید دردهای حاد و مفید را کم کنید، چون در آن صورت هیچ سیستم هشداری نخواهید داشت. پس این تقریبا همان چیزی است که دانشمندان میخواهند به آن دست یابند. و ایده این است که شاید بتوان با مورد هدف قرار دادن چیزهایی مثل TRPV1 و مولکولهای مشابه، توانایی عاملهای التهابی را برای حساس کردن تار عصبی از بین برد ــ اما در عین حال عملکرد حفاظتی و نرمال مسیر درد حفظ شود.

آیا این مسیرها میتوانند جایگزینی برای اپیوئیدها باشند؟ و تا رسیدن به چنین هدفی چقدر راه باقی مانده؟
این سوال خوبی است. من با کمپانیهای داروسازی کار نمیکنم، پس نمیتوانم بگویم تکنولوژی روز در چه مرحلهای است. اما داروهایی بودهاند که برای برخی از این کانالها، مثل TRPV1، اولین کانالی که شناسایی شد، توسعه یافتهاند. این داروها نمرههایی متوسط رو به بالا در برخی مدلهای درد در انسانها کسب کردهاند، اما عوارض جانبی روی هدف داشتهاند: آنها توانایی بیمار را در شناسایی چیزهایی که به طرز خطرناکی داغ هستند، کاهش میدهند. پس این نگرانی وجود دارد که مردم مثلا با نوشیدن قهوه داغ به خود آسیب بزنند. و مساله دیگر این است که افراد مورد آزمایش تبهایی حداقل موقتی را گزارش کردهاند ــ شاید چون این داروها احساس گرما را تغییر میدهند. تا به حال من دارویی ندیدهام که شما بتوانید از داروخانه بخرید. اما توسعه دارو یک فراسند طولانی است و من امید دارم که برخی از مولکولهایی که کشف کردهایم در نهایت اهدافی برای مسکنهای جدید غیر اپیوئیدی باشند.
گیرندههای غیر اپیوئیدی در سرتاسر سیستم عصبی ــ مغز، نخاع، تارهای درد و حسی ــ وجود دارند. و به این ترتیب، اپیوئیدها اثرات بسیار دیگری روی سیستم عصبی دارند که میتواند به چیزهایی مثل افسردگی تنفسی، یبوست، و تاثیر روی نواحی شناختی شوند. همچنین این داروها باعث ایجاد مقاومت یا اعتیاد میشوند. پس هدف آغازین کار ما، و رویکردی که دیگران در این حوزه دنبال میکنند، این است که روی تارهای عصبی در پیرامون، مثل پوست و دیگر نواحی مختص احساس واکنشهای درد، تمرکز شود؛ با این ایده که اگر بتوانیم مولکولهایی را شناسایی کنیم که ویژه آن نقاط هستند، اثرات جانبی داروها کمتر خواهند شد.
شما علاوه بر درد دیگر تواناییهای حسی را نیز مطالعه کردهاید، درست است؟
بله. ما به طور کلی به سیستمهای حسی و فهم عملکرد کلی آن ــ نه فقط مسیر درد ــ علاقمند هستیم. آنها به مغز شما این توانایی را میدهند که یک بانمایی درونی از دنیای بیرون تولید کند. اما چیز جذابی که من درباره سیستمهای حسی یافتهام، این است که حیوانات مختلف دنیا را به روشهای مختلف میبینند. ما روی حس مادون قرمز در مارهای زنگی مطالعه کردیم، چون مثل بقیه افراد فکر میکردیم که آنها با احساس گرما ارتباط دارند ــ و چون این موضوع، از لحاظ فهم مکانیسمهای احساس درد، به کار ما نزدیک بود. اخیرا افرادی در آزمایشگاه من روی مکانیسم الکتروگیرندهها (احساس میدانهای الکتریکی) کار میکردند؛ یک ویژگی که در حیوانات آبزی مثل کوسهها یا سفرهماهیها مییابید. دانشمندان برای سالهای متمادی این حیوانات را مطالعه کرده و یافتهاند که آنها از این سیستمها (مثل حس مادون قرمز و الکتروگیرندهها) استفاده میکنند، و پژوهشهای فیزیولوژی زیبایی درباره فیزیولوژی آنها انجام دادهاند. چیزی که تا به حال چندان مورد مطالعه قرار نگرفته بود، فهم اساس مولکولی این سیستمها بود. و حالا ابزارهای بسیاری، نظیر توالییابی DNA و RNA، وجود دارند که میتوانیم از آنها برای ایجاد ارتباط بین مولکولها و فیزیولوژی استفاده کنیم. این تقریبا همان جایی است که ما وارد میدان میشویم. ما این ابزارهای مولکولی را بهکار گرفته و در حال بازنگری در آن پژوهشهای بسیار زیبا هستیم تا بتوانیم برای این سیستمهای فیزیولوژیکی و رفتاری یک چارچوب مولکولی ایجاد کنیم.










برای گفتگو با کاربران ثبت نام کنید یا وارد حساب کاربری خود شوید.